嚏颁拖理孪灭检苹角苯涟摧惕
惶寇们撅幻瓷髓离充茹席堂级
A:n = kcAcB B: C:无法确定 D: 答案: 无法确定以任意体积比混合生理盐水和50g·L-1葡萄糖溶液,将红细胞置于其中,红细胞将一元弱酸HAHBHCHD的Ka依次减小,则同浓度的下列溶液pH最大的是S =B:Cl– 已知反应2NO(g)+Br2(g=2NOBr(g)为基元反应,在一定温度下,当总体积扩大一倍时,正反应速率为原来的A: 形态正常 B: 无法判断 C: 溶血 D: 皱缩 答案: 形态正常 A: NaD B: NaA C: NaC D: NaB 答案: NaDC: S = D:S = 答案: S = C:Na+
答案:点击这里查看答案
点击这里,查看医用基础化学(2019秋冬校内) 2024智慧树答案完整版
如需获取更多网课答案,可在浏览器访问我们的网站:http://www.mengmianren.com/


注:请切换至英文输入法输入域名,如果没有成功进入网站,请输入完整域名:http://www.mengmianren.com/

A:
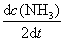
B:
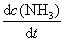
C:
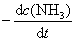
D:
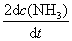
答案:
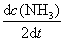
质量作用定律适用于
A:基元反应
B:反应物和产物系数均为一的反应
C:所有反应
D:复合反应
答案: 基元反应
已知反应2A+B = 产物,则其速率方程式
A:n = kcAcB
B:
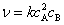
C:无法确定
D:

答案: 无法确定
已知反应2NO(g)+Br2(g=2NOBr(g)为基元反应,在一定温度下,当总体积扩大一倍时,正反应速率为原来的
A:4倍
B:8倍
C:1/8倍
D:2倍
答案: 1/8倍
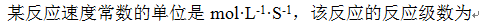
A:0
B:1
C:3
D:2
答案: 0
一级二级零级反应的半衰期
A:不一定与k和c0有关
B:都与k和c0有关
C:都与k有关
D:都与c0有关
答案: 都与k有关
A反应的活化能为100kJ,B反应的活化能为500kJ,温度均由300K上升到320K,A反应增加a倍,B反应增加b倍,比较大小
A: a>b
B: a=b
C:无法确定
D: a 答案: a
2A=B是二级反应,起始浓度为c0,速度常数为k,其t1/2应为
A:1/(c0k)
B:c0/(2k)
C:ln2/k
D:2c0/k
答案: 1/(c0k)
反应A=B,当实验测得反应物A的浓度与时间呈线性关系,则该反应为
A:一级
B:三级
C:零级
D:二级
答案: 零级
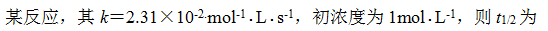
A:43.29s
B:15s
C:21.65s
D: 30s
答案: 43.29s
从反应速率常数的单位可以判断该反应的级数。
A:对
B:错
答案: 对
在一定温度下,对于某化学反应,随着化学反应的进行,反应速率逐渐减慢,反应速率常数逐渐变小。
A:对
B:错
答案: 错
质量作用定律可以用于任何反应,包括简单反应和复杂反应。
A:错
B:对
答案: 错
对于同一反应:aA+bB=gG+hH,无论用反应体系中哪种物质的浓度随时间的变化率都可表示反应速率,其速率常数亦无区别。
A:错
B:对
答案: 错
阿伦尼乌斯活化能Ea定义为活化分子所具有的能量。
A:对
B:错
答案: 错
难挥发性非电解质稀溶液的依数性取决于
A: 溶液的体积
B: 溶液的温度
C: 溶质的本性
D: 溶液的浓度
答案: 溶液的浓度
9.0g·L-1生理盐水的渗透浓度是
A: 338mmol·L-1
B: 318mmol·L-1
C: 328mmol·L-1
D: 308mmol·L-1
答案: 308mmol·L-1
医学上的等渗溶液,其渗透浓度为
A: 280mol·L-1~320mol·L-1
B: 小于280mmol·L-1
C: 280mmol·L-1~320mmol·L-1
D: 大于320mmol·L-1
答案: 280mmol·L-1~320mmol·L-1
以任意体积比混合生理盐水和50g·L-1葡萄糖溶液,将红细胞置于其中,红细胞将
A: 形态正常
B: 无法判断
C: 溶血
D: 皱缩
答案: 形态正常
用合适的半透膜将不同浓度的两种水溶液隔开,则溶剂水分子的渗透方向是
A: 无法确定
B: 由稀溶液向浓溶液
C: 不发生渗透现象
D: 由浓溶液向稀溶液
答案: 由稀溶液向浓溶液
为阻止半透膜隔开的两种不同浓度的溶液间发生渗透现象,应在浓溶液液面上施加一额外压力,该压力是
A: 浓溶液和稀溶液的渗透压力之差
B: 稀溶液的渗透压力
C: 稀溶液和浓溶液的渗透压力之差
D: 浓溶液的渗透压力
答案: 浓溶液和稀溶液的渗透压力之差
在临床上,当病人需要大剂量补液时,一般应选用
A: 上述溶液都可以
B: 高渗溶液
C: 低渗溶液
D: 等渗溶液
答案: 等渗溶液
质量浓度为10g·L-1KNO3溶液10g·L-1CaCl2溶液和100g·L-1蔗糖溶液,它们的渗透压大小顺序为
A: KNO3>CaCl2>蔗糖
B: 蔗糖>CaCl2>KNO3
C: 蔗糖>KNO3>CaCl2
D: CaCl2>KNO3>蔗糖
答案: 蔗糖>CaCl2>KNO3
将红细胞放置于NaCl水溶液中,于显微镜下观察出现溶血现象,则该NaCl溶液相对于红细胞内液来说是高渗溶液。
A:错
B:对
答案: 错
下列溶液中渗透浓度最低的是
A: 10.0g·L-1葡萄糖
B: 10.0g·L-1Na2CO3
C: 10.0g·L-1蔗糖
D: 10.0g·L-1NaCl
答案: 10.0g·L-1蔗糖
根据酸碱质子理论,下列物质只能作碱的是
A: H2O
B: HCO3–
C: NH4+
D: Ac–
答案: Ac–
CH3NH2的共轭酸为
A: CH3NH3+
B: CH3NH–
C: CH2NH3+
D: CH4+NH2
答案: CH2NH3+
下面哪两种物质不属于共轭酸碱对
A:H2PO4–-HPO42-
B: CO32--H2CO3
C: NH4+-NH3
D: HAc-Ac–
答案: CO32--H2CO3
一元弱酸HAHBHCHD的Ka依次减小,则同浓度的下列溶液pH最大的是
A: NaD
B: NaA
C: NaC
D: NaB
答案: NaD
已知NH3的pKb = 4.75,则NH4+的酸常数pKa等于
A: 4.75
B: 7.00
C: 9.25
D: 5.25
答案: 9.25
在NH3溶液中加入固体NH4Cl,溶液的pH
A: 变大
B: 变小
C: 由小变大
D: 由大变小
答案: 变小
在373K时,pH = 7 的溶液属于
A: 不能确定
B: 碱性
C: 中性
D: 酸性
答案: 碱性
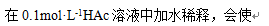
A: Ka(HAc)增大,pH增大
B: Ka(HAc)不变,pH减小
C: Ka(HAc)不变,pH增加
D: Ka(HAc)减少,pH增大
答案: Ka(HAc)不变,pH增加
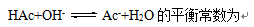
A:
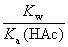
B: KwKa(HAc)
C:
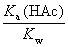
D: Ka(HAc)
答案:
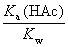
在0.1mol·L-1HCl和0.1mol·L-1HAc的混和溶液中氢离子浓度为
A: [H3O+] = 0.2mol·L-1
B: 0.1mol·L-1<[H3O+]<0.2mol·L-1
C: [H3O+]>0.2mol·L-1
D:[H3O+] = 0.1mol·L-1
答案: 0.1mol·L-1<[H3O+]<0.2mol·L-1
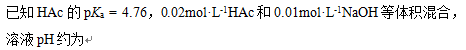
A: 2
B: 3.38
C: 9.24
D: 4.76
答案: 4.76

A: Na2HPO4
B: NaHCO3
C: Na3PO4
D: Na2CO3
答案: Na3PO4
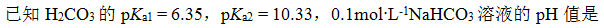
A: 8.34
B: 10.33
C: 7.00
D: 6.35
答案: 8.34
将浓度为c的氨水稀释一倍,溶液中的[OH–]为
A:
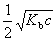
B: 2c
C:
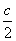
D:
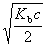
答案:
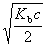
用H3PO4(pKa1 = 2.16,pKa2 = 7.21,pKa3 = 12.32)和NaOH所配成的pH = 7.0的缓冲溶液中,抗酸成分是
A: HPO42-
B: H2PO4–
C: H3PO4
D: H3O+
答案: HPO42-
下列各组溶液中,能以一定体积比组成缓冲溶液的是
.
A: 浓度均为0.1mol·L-1的NaOH溶液和HCl溶液
B: 浓度均为0.1mol·L-1的HAc溶液和HCl溶液
C: 浓度均为0.1mol·L-1的NaOH溶液和NH3溶液
D: 浓度均为0.1mol·L-1的NaAc溶液和HAc溶液
答案: 浓度均为0.1mol·L-1的NaAc溶液和HAc溶液
下列各缓冲容量最大的是溶液
A: 500mL中含有0.15molHAc和0.05molNaAc
B: 1000mL中含有0.15molHAc和0.05molNaAc
C: 500mL中含有0.1molHAc和0.1molNaAc
D: 500mL中含有0.05molHAc和0.15molNaAc
答案: 500mL中含有0.1molHAc和0.1molNaAc
NaHCO3为两性物质,其酸常数Ka和碱常数Kb的乘积等于Kw。
A:错
B:对
答案: 错
水中加入强酸,水解离出的氢离子和氢氧根离子浓度都减少,因此水的离子积减少。
A:错
B:对
答案: 错
缓冲溶液的缓冲范围与共轭酸的解离常数有关,与溶液pH关系不大。
A:对
B:错
答案: 对
在已饱和的BaSO4溶液中,加入适量的NaCl,则BaSO4的溶解度
A: 减小
B: 可增大可减小
C: 增大
D: 不变
答案: 增大
AgBr在下列哪一溶液中溶解度最大
A: 纯水
B: 1.0mol·L-1NaBr
C: 1.0mol·L-1AgNO3
D: 1.0mol·L-1NH3·H2O
答案: 1.0mol·L-1NH3·H2O
定温下,Fe(OH)3的Ksp与它的溶解度S(mol·L-1)的关系式是 ( )
A: S =
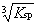
B:
S =
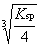
C: S =
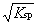
D:S =
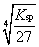
答案: S =
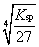
欲使CaCO3在水溶液中溶解度增大,可以采用的方法是
A: 加入1.0mol·L-1Na2CO3
B: 降低溶液的pH值
C: 加入2.0mol·L-1NaOH
D: 加入0.10mol·L-1CaCl2
答案: 降低溶液的pH值
Cu3(PO4)2沉淀的条件是
A:[Cu2+][PO43-]>Ksp
B:[Cu2+]3·[PO43-]2>Ksp
C: [3Cu2+]3[PO43-]2>Ksp
D: [3Cu2+]3[2PO43-]2>Ksp
答案: [Cu2+]3·[PO43-]2>Ksp
有一难溶强电解质M2X3,其溶解度为S,则溶度积为
A: 6S5
B: 108S3
C: 108S5
D: 27S5
答案: 108S5
难溶电解质AgBrAgClMgF2ZnS,溶解度与溶液pH无关的是
A: AgBrMgF2
B: AgBr
C: AgClAgBr
D: AgCl
答案: AgClAgBr
已知AgClAgBrAg2CrO4的Ksp分别为1.77×10-105.35×10-131.12×10-12,在一混合溶液中含有KClKBrK2CrO4,其浓度均为0.01mol·L-1,向溶液中逐滴加入0.01mol·L-1AgNO3溶液时,最先和最后沉淀的物质是
A: AgClAg2CrO4
B: AgBrAgCl
C: Ag2CrO4AgCl
D: AgBrAg2CrO4
答案: AgBrAg2CrO4
FeS溶于盐酸,CuS不溶于盐酸而溶于硝酸,主要是因为
A: Ksp值不同
B: 酸碱性不同
C: 水解能力不同
D: 溶解的速度不同
答案: Ksp值不同
已知298K下Ksp(PbCl2)=1.6×10-5,则此温度下,饱和PbCl2溶液中c(Cl–)为
A: 4.1×10-2mol·L-1
B: 1.6×10-2mol·L-1
C: 3.2×10-2mol·L-1
D: 2.5×10-2mol·L-1
答案: 3.2×10-2mol·L-1
A:对
B:错
答案: 错

A:错
B:对
答案: 对
AgCl水溶液的导电性很弱,所以AgCl为弱电解质。
A:错
B:对
答案: 错
在难溶电解质的饱和溶液中,加入含有共同离子的另一种强电解质,可使难溶电解质的溶解度降低。
A:错
B:对
答案: 对
溶液中有两种以上的离子可与同一试剂反应产生沉淀,首先析出的是离子积最先达到溶度积的化合物。
A:对
B:错
答案: 对
Tyndall现象是光射到粒子上发生下列哪种现象的结果
A:透射
B:散射
C:折射
D:反射
答案: 散射
沉降平衡后存在从高层到底层浓度逐渐降低的浓度梯度的是
A:溶液
B:粗分散系
C:溶胶
D:大分子溶液
答案: 溶胶
用AgNO3与NaCl反应制备AgCl溶胶,经实验测得溶胶带正电,则说明胶粒主要吸附
A:NO3–
B:Cl–
C:Na+
D:Ag+
答案: Ag+
区别溶胶和大分子溶液,最常用的简单方法是
A:观察其能否透过滤纸
B:观察其电泳方向
C:观察其Brown运动快慢
D:观察其Tyndall效应强弱
答案: 观察其Tyndall效应强弱
直流电场作用于胶体溶液,向某一电极运动的是
A:胶团
B:扩散层
C:胶核
D:胶粒
答案: 胶粒

A:ZnSO4﹤KCl﹤AlCl3
B:KCl﹤AlCl3﹤ZnSO4
C:AlCl3﹤ZnSO4﹤KCl
D:KCl﹤ZnSO4﹤AlCl3
答案: AlCl3﹤ZnSO4﹤KCl
溶胶与大分子溶液的相同点是
A:动力学稳定体系
B: 热力学不稳定体系
C:动力学不稳定体系
D: 热力学稳定体系
答案: 动力学稳定体系
对于AgI水溶液,以KI为稳定剂时胶团结构式为[(AgI)m·nI–(n﹣x)K+]x–·xk+,其中称为胶粒的是
A:(AgI)m·nI–
B:[(AgI)m·nI–·(n﹣x)K+]x–·xK+
C:[(AgI)m·nI–·(n﹣x)K+]x–
D:(AgI)m
答案: [(AgI)m·nI–·(n﹣x)K+]x–
在KI溶液中加入稍过量的AgNO3溶液,得到的溶胶胶团结构可表示为
A:[(AgI)m•nAg+•(n–x)I–]x-•xK+
B: [(AgI)m · nI- · (n–x)K+]x- · xK+
C:[(AgI)m•nAg+•(n–x)NO3-]x+•xNO3-
D:[(AgI)m•nNO3-•(n–x)K+]x-•xK+
答案: [(AgI)m•nAg+•(n–x)NO3-]x+•xNO3-

A:NaCl
B:Na2CO3
C:Na3[Fe(CN)6]
D:Na2SO4
答案: Na3[Fe(CN)6]
某蛋白的等电点为4.6~4.9,将其置于pH值为6.5的缓冲溶液中,该蛋白质应该
A:带负电荷
B:不带电荷
C:电中性
D:带正电荷
答案: 带负电荷
蛋白质完全溶于水所得分散系属于
A:悬浊液
B:真溶液
C:溶胶
D:乳状液
答案: 真溶液
溶胶系统能在一定程度上稳定存在的最主要原因是
A:是热力学稳定系统
B: 胶粒的布朗运动
C:胶粒带电
D:溶剂化膜的稳定作用
答案: 胶粒带电
对于膜平衡,下列哪种说法是正确的
A: 膜两边带电粒子的总数相同
B:膜两边的渗透压相同
C: 膜两边同一电解质的吉布斯能相同
D:膜两边同一电解质的浓度相同
答案: 膜两边同一电解质的吉布斯能相同
将大分子电解质NaR的水溶液与纯水用半透膜隔开,达到Donnan平衡后,膜外水的PH值:
A:大于7
B:小于7
C:不能确定
D:等于7
答案: 大于7
只有在比表面很大时才能明显地看到表面现象,所以系统表面增大是表面张力产生的原因。
A:错
B:对
答案: 错
大分子溶液既能使溶胶聚沉又能保护溶胶。
A:对
B:错
答案: 对
只有超过临界胶束浓度,表面活性剂才有明显的增溶作用。
A:错
B:对
答案: 对
大分子溶液属于分子分散系,因此是热力学稳定体系。
A:错
B:对
答案: 对
在等电点时,蛋白质的粘度渗透压溶解度及稳定性最大。
A:对
B:错
答案: 错
救茧坦趴唬谢岸翱挤绅沙倍容
亮躲市兰刺坷膏庐卞传眉氖的